
产品中心
Red Blood Cell Lysis Solution
高通量单细胞测序对单细胞悬液质量要求很高,除了细胞活性等参数外,单细胞悬液的有核率是影响后续数据质量的重要因素,较低的有核率可能引起有效细胞识别不准确、有效细胞及非细胞界限模糊、捕获细胞数过高或过低,背景升高等不利现象。红细胞含量过多是造成有核率低的重要原因之一。
百奥益康团队累积了10,000+个样本的单细胞测序服务经验,涉及150+种不同类型的组织,具有丰富的新鲜组织解离的经验。在此基础上,百奥益康自主研发了红细胞裂解液,利用该裂解液,可高效的裂解单细胞悬液中的红细胞,提高悬液质量。
产品优势

适用范围:哺乳动物细胞悬液中红细胞的快速高效裂解。
性能表现:可快速、高效的裂解单细胞悬液中的红细胞,同时几乎不伤害其他淋巴细胞或其他有核的细胞,大幅度改善单细胞悬液质量,从而获得该高质量的数据结果。
应用场景:适用于含有大量红细胞的细胞悬液优化,可应用于高通量单细胞测序等相关科学研究实验。
测试效果
我们对新鲜的人PBMC进行了实验,从细胞直径分布图可以看出,红细胞裂解处理后,红细胞的分布明显减少,单细胞悬液的有核率参数也从32.4%提升至92.6%,并且活性也得到明显改善。从数据分析结果可以看出,红细胞裂解处理后,测得的基因中位数明显改善,从497提升至1,666。
测试流程:
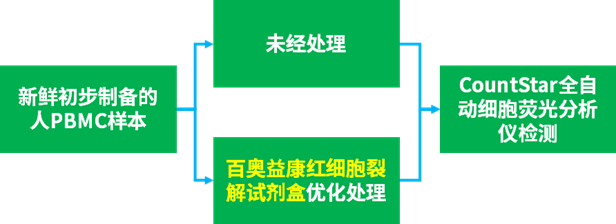
测试结果:
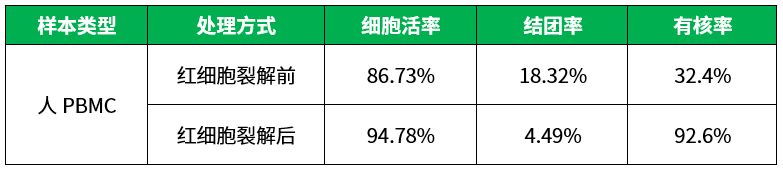
人PBMC样本经过红细胞裂解液处理前后样本质检结果对比
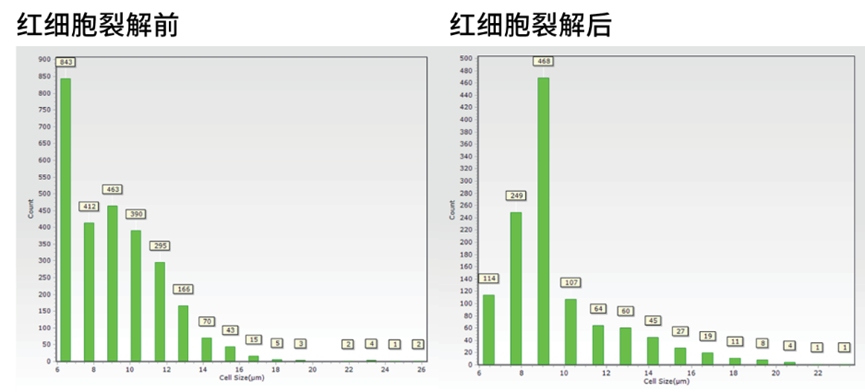
人PBMC样本经过红细胞裂解液处理前后样本细胞直径分布
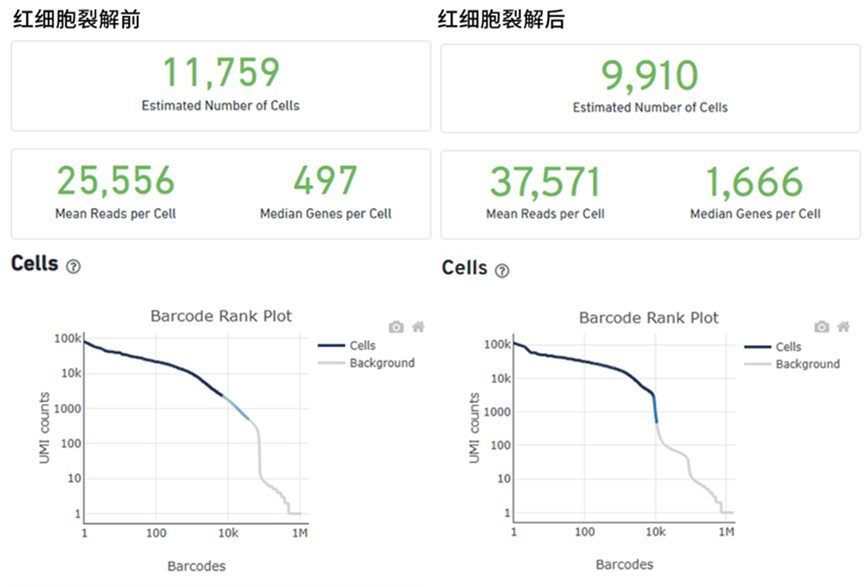
人PBMC样本经过红细胞裂解液处理前后样本测序数据结果对比
注:以上数据均经对应项目的客户同意后发布。
产品说明书
点击下载:百奥益康红细胞裂解液使用说明书(货号:BA3311)
订购信息
BA3311,红细胞裂解液,100 mL,¥150
相关产品
百奥益康样本保存系列试剂盒:
BA3301,动物组织通用保存液,100 mL,¥1,200
BA3313,胰腺组织保存液,4 rxns,¥2,000
BA3312,动物组织冻存液,100 mL,¥2,500
BA3309,通用细胞冻存液,100 mL,¥800
BA3341,无血清无DMSO细胞冻存液,100 mL,¥1,200
百奥益康细胞核悬液制备系列试剂盒:
BA3302,动物组织细胞核悬液制备试剂盒,10 rxns,¥3,000
BA3315,肌肉组织细胞核悬液制备试剂盒,10 rxns,¥3,500
BA3342,脂肪组织细胞核悬液制备试剂盒,10 rxns,¥3,500
BA3343,血管组织细胞核悬液制备试剂盒,10 rxns,¥3,500
BA3319,植物组织通用细胞核悬液制备试剂盒,10 rxns,¥4,000
百奥益康细胞悬液制备系列试剂盒:
BA3303,哺乳动物组织通用解离试剂盒,10 rxns,¥2,500
BA3344,通用外周血单个核细胞(PBMC)分离液(沉降法),100 mL,¥300
BA3331,小鼠外周血单个核细胞(PBMC)分离液,100 mL,¥500
BA3332,人外周血单个核细胞(PBMC)分离液,100 mL,¥500
BA3333,人骨髓血单个核细胞(BMMC)分离液,100 mL,¥500
BA3305,小鼠脑组织解离试剂盒,10 rxns,¥3,000
BA3326,人脑组织解离试剂盒,10 rxns,¥3,000
BA3307,皮肤组织解离试剂盒,10 rxns,¥2,000
BA3340,小鼠皮肤组织解离试剂盒,10 rxns,¥2,000
BA3308,骨组织解离试剂盒,10 rxns,¥4,000
BA3310,血管组织解离试剂盒,10 rxns,¥9,000
BA3337,血管组织解离试剂盒(Plus),10 rxns,¥12,000
BA3314,胰腺组织解离试剂盒,4 rxns,¥6,000
BA3320,肿瘤组织解离试剂盒,10 rxns,¥2,000
BA3321,耳蜗组织解离试剂盒,10 rxns,¥4,000
BA3322,肾脏组织解离试剂盒,10 rxns,¥2,500
BA3323,肝脏组织解离试剂盒,10 rxns,¥2,500
BA3324,脾脏组织解离试剂盒,10 rxns,¥2,000
BA3325,肺脏组织解离试剂盒,10 rxns,¥2,000
BA3327,心脏组织解离试剂盒,10 rxns,¥5,000
BA3328,气管组织解离试剂盒,10 rxns,¥4,000
BA3316,胃肠道组织解离试剂盒,10 rxns,¥5,000
BA3334,脊髓组织解离试剂盒,10 rxns,¥4,000
BA3336,输卵管组织解离试剂盒,10 rxns,¥5,000
BA3335,环节动物组织解离试剂盒,10 rxns,¥6,000
BA3317,植物组织通用原生质体悬液制备试剂盒,10 rxns,¥6,000
百奥益康细胞悬液优化系列试剂盒:
BA3311,红细胞裂解液,100 mL,¥150
BA3345,抗细胞结团剂,100 mL,¥1,500
BA3338,死细胞去除缓冲液,10 rxns,¥2,000
BA3339,死细胞碎片杂质去除试剂盒,10 rxns,¥4,000
BA3329,消化系统组织细胞碎片去除试剂盒,10 rxns,¥4,000
BA3330,脑组织细胞碎片去除试剂盒,10 rxns,¥2,000